Die Aktivität des Herzmuskels wird durch ein komplexes anatomisches System mit unterschiedlichen äußeren Einflussfaktoren elektrisch gesteuert. Schrittmacherzellen erzeugen einen elektrischen Reiz, der über elektrische Leitungsbahnen durch das Herz geleitet wird und sich anschließend von einer Herzmuskelzelle zur nächsten überträgt, bis alle Zellen erregt worden sind. Außerhalb des Reizleitungssystems geschieht dies über Gap Junctions, die Kardiomyozyten miteinander verbinden und eine direkte Übertragung des elektrischen Reizes zwischen zwei Zellen ermöglichen. Es wird ein sogenanntes funktionelles Synzytium geschaffen, was bedeutet, dass ein Reiz immer den gesamten Herzmuskel Herzmuskel Anatomie des Herzens erregt und somit auch kontrahiert (Alles-oder-Nichts-Gesetz). Die elektrischen Reize an sich werden durch den Fluss geladener Teilchen über die Zellmembran Zellmembran Die Zelle: Zellmembran von Kardiomyozyten generiert. Dieser Fluss verändert die Spannung, die an der Membran anliegt und öffnet spezialisierte, spannungsabhängige Ionenkanäle, wodurch sich das Signal weiter ausbreiten kann. Über Rezeptoren Rezeptoren Rezeptoren des vegetativen Nervensystems am Herzen werden ebenfalls bestimmte Ionenkanäle geöffnet oder geschlossen, was sich vor allem in einer Änderung der Herzfrequenz auswirkt.
Kostenloser
Download
Lernleitfaden
Medizin ➜
Sinusknoten (lat. Nodus sinoatrialis, Abkürzung: SA):
Atrioventrikularknoten (Abkürzung: AV-Knoten):
His-Bündel His-Bündel Anatomie des Herzens und Purkinje-Fasern Purkinje-Fasern Anatomie des Herzens:

Reizleitungssystem und autonome Schrittmacher:
Lage der Schrittmacherzellen im Reizleitungssystem des Herzens und ihre entsprechenden autonomen Rhythmen
Kardiomyozyten ohne Schrittmacherfunktion:

Ablauf der Erregungsausbreitung des Herzens
AV: atrioventrikulär
Aktionspotentiale bewegen sich mit unterschiedlicher Geschwindigkeit durch verschiedene Gewebe und Bestandteile des Reizleitungssystems.
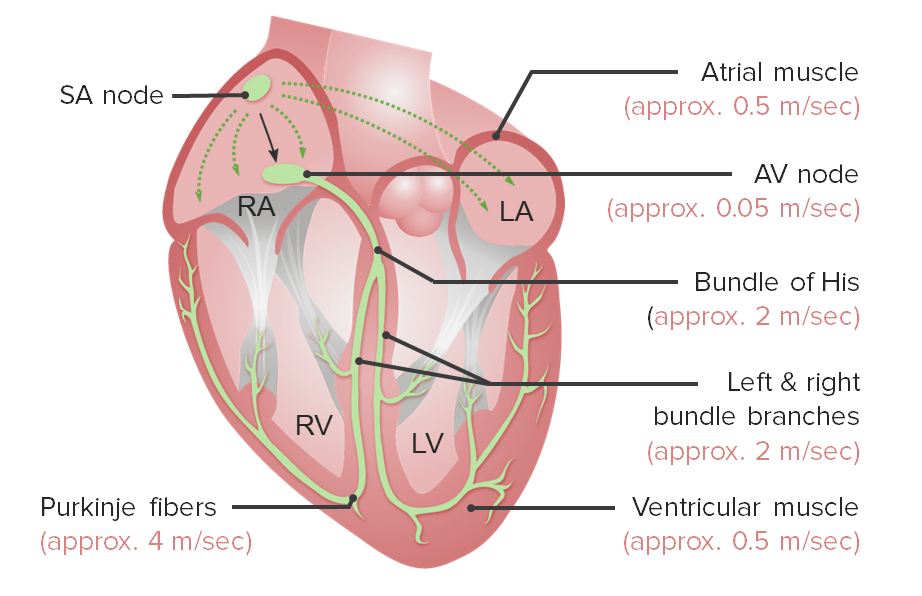
Reizleitungssystem und Leitungsgeschwindigkeiten seiner Bestandteile
SA: sinoatrial
AV: atrioventrikulär
RV: rechter Ventrikel
LV: linker Ventrikel
RA: rechtes Atrium
LA: linkes Atrium
Herzmuskelzellen des Arbeitsmyokards depolarisieren nur, wenn sie ein elektrischer Reiz erreicht. Ohne Stimulation befinden sie sich in einem Ruhezustand und haben ein Ruhemembranpotential Ruhemembranpotential Membranpotenzial.

Ionentransport bei Ruhepotential:
Beim hyperpolarisierten Ruhepotential sind spannungsgesteuerte K+-Kanäle die einzigen offenen Kanäle; daher stabilisiert K+ in erster Linie das Ruhemembranpotential der Zellen.

Depolarisation der Kardiomyozyten:
Die Ausbreitung von Aktionspotentialen erfolgt durch Gap Junctions, die Kardiomyozyten miteinander verbinden. Sie beeinflussen so die Öffnung spannungsgesteuerter Na+– und Ca2+-Kanäle.
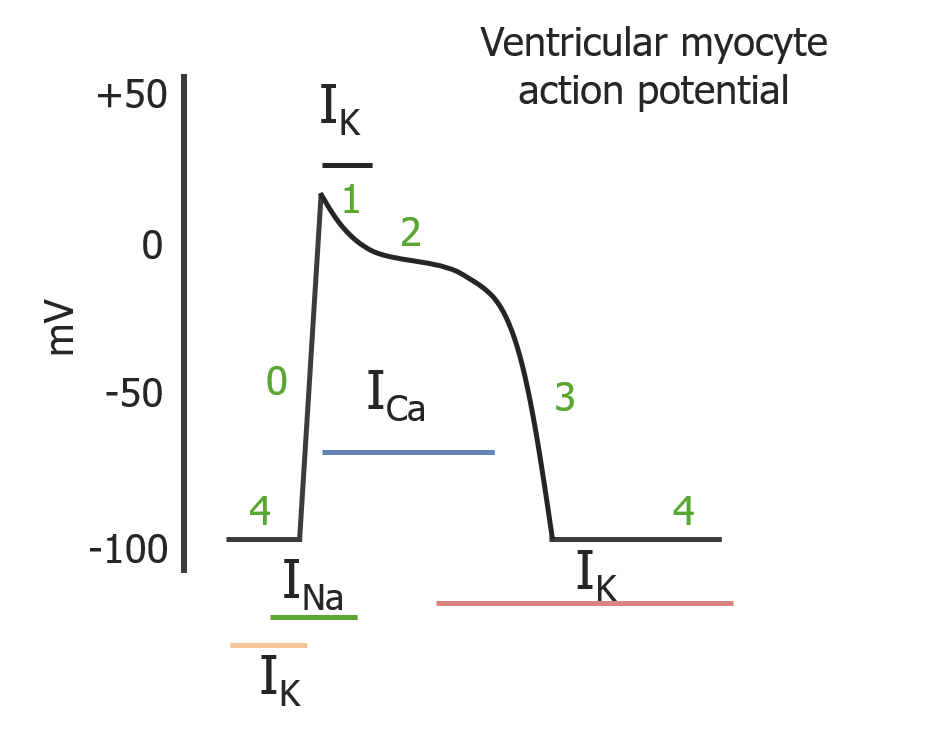
Phasen eines Aktionspotentials von Herzmuskelzellen:
Die Phasen 0, 1, 2, 3 und 4 treten nacheinander auf. Die farbigen Linien stellen die Dauer der jeweiligen Ionenströme dar.
IK: K+-Strom
ICa: Ca2+-Strom
INa: Na+-Strom
| Kanal | Phase 4 | Phase 0 | Phase 1 | Phase 2 | Phase 3 |
|---|---|---|---|---|---|
| Spannungsgesteuerte Na+-Kanäle | – | Offen | Schließen sich | – | – |
| Schnelle K+-Kanäle | – | – | Offen | – | – |
| L-Typ-Ca2+-Kanäle | – | – | Öffnen sich | Offen | Schließen sich |
| Verzögerte K+-Kanäle | Offen | – | – | – | Offen |

Herzmuskelzellen sind über Gap Junctions miteinander verbunden. Die Depolarisation breitet sich über Gap Junctions aus.
Bild von Lecturio.
Gap Junctions zwischen Herzmuskelzellen
Bild von Lecturio.Schrittmacherzellen, die sich in den SA- und AV-Knoten befinden, unterliegen ständigen Änderungen des Aktionspotentials und besitzen somit kein typisches Ruhepotential.

Phasen eines Aktionspotentials einer Schrittmacherzelle:
Die Phasen 4, 0, 3 und 4 treten nacheinander auf. Die farbigen Linien stellen die Dauer der jeweiligen Ionentröme dar.
If : „funny“ Ionenstrom
ICa(T): vorübergehender, kurzer Ca2+-Strom
ICa(L): lang anhaltender Ca2+-Strom
IK: K+-Strom
| Kanaltyp | Phase 4 | Phase 0 | Phase 3 |
|---|---|---|---|
| HCN-Kanal | Offen* | – | – |
| Transiente oder T-Typ-Ca2+-Kanäle | Offen | Geschlossen | – |
| L-Typ-Ca-2+-Kanäle | – | Offen | Geschlossen |
| Verzögerte K+-Kanäle | Offen | – | Offen |
Im Vergleich zum Arbeitsmyokard haben Aktionspotentiale von Schrittmacherzellen die folgenden Eigenschaften:

Aktionspotentiale von Schrittmacherzellen (grün) und Arbeitsmyokard (rot):
Aktionspotentiale am Arbeitsmyokard beginnen mit einer schnellen Depolarisation, gefolgt von einer langsamen Repolarisation, während Aktionspotentiale von Schrittmacherzellen eine längere Depolarisationsphase haben. Aktionspotentiale des Arbeitsmyokard gehen ebenfalls von einer isoelektrischen (flachen) Linie aus, während Aktionspotentiale von Schrittmacherzellen diese durch den ständigen Wechsel zwischen De- und Repolarisation nicht besitzen.
Unter Chronotropie versteht man die Beeinflussung der Geschwindigkeit der Erregung auf der Ebene der Schrittmacherzellen und somit die Herzfrequenz. Die Frequenz des SA-Knotens wird hauptsächlich vom vegetativen bzw. autonomen Nervensystem Nervensystem Nervensystem: Aufbau, Funktion und Erkrankungen (Abkürzung: VNS/ANS) und speziell dem Sympathikus und Parasympathikus beeinflusst.
Dromotropie ist die Beeinflussung der Leitungsgeschwindigkeit durch den AV-Knoten (auch vom VNS kontrolliert):

Autonome Regulierung der HF am SA-Knoten:
Das sympathische Nervensystem erhöht die HF (positive Chronotropie), indem es über die β1-adrenergen Rezeptoren des SA-Knotens eingreift. Das parasympathische Nervensystem verringert die HF (negative Chronotropie) über den Nervus vagus, indem es über die muskarinischen Rezeptoren (M2) am SA-Knoten einwirkt.
Cholinerge Nerven setzen Acetylcholin frei, welches vorwiegend zwei Veränderungen an den Myozyten Myozyten Arten von Muskelgewebe bewirkt:

Parasympathische Beeinflussung der HF über den AV-Knoten
AV: atrioventrikulär
AP: Aktionspotential
Vm: Membranpotential
HCN: hyperpolarization-activated cyclic nucleotide-gated
Noradrenalin wird von sympathischen Nerven freigesetzt, bindet an β1-adrenerge Rezeptoren Rezeptoren Rezeptoren der Myozyten Myozyten Arten von Muskelgewebe und bewirkt einen intrazellulären Anstieg von cAMP. Dadurch erhöht sich die HF über zwei Mechanismen:

Sympathische Beeinflussung der HF über den AV-Knoten
AV: atrioventrikulär
AP: Aktionspotential
Vm: Membranpotential
HCN: hyperpolarization-activated cyclic nucleotide-gated
| Einflussfaktor | Erhöhung HF (positive Chronotropie) | Verminderung HF (negative Chronotropie) |
|---|---|---|
| VNS* | Sympathisches Nervensystem Nervensystem Nervensystem: Aufbau, Funktion und Erkrankungen | Parasympathisches Nervensystem Nervensystem Nervensystem: Aufbau, Funktion und Erkrankungen |
| Schilddrüsenhormone Schilddrüsenhormone Schilddrüsenhormone | Hyperthyreose Hyperthyreose Thyreotoxikose und Hyperthyreose | Hypothyreose Hypothyreose Hypothyreose |
| K+ | Hypokaliämie | Hyperkaliämie Hyperkaliämie Hyperkaliämie |
| Katecholamine im Kreislauf |
|
– |
| Durchblutung/O2-Angebot | – | Ischämie/Hypoxie |
Blockierungen im Bereich des AV-Knotens bedeuten, dass eine anatomische oder funktionelle Beeinträchtigung des Reizleitungssystems des Herzens eine Verzögerung oder Unterbrechung der Übertragung von Aktionspotentialen von den Vorhöfen auf die Ventrikeln auf Höhe des AV-Knotens verursacht. Betroffene Personen können asymptomatisch sein oder sich je nach Schwere der Blockade mit Synkopen, Brustschmerzen Brustschmerzen Brustschmerzen, Dyspnoe Dyspnoe Dyspnoe (Atemnot/Luftnot), Bradykardie Bradykardie Bradyarrhythmien sowie Bewusstseinsstörungen präsentieren. Mittels eines EKGs wird die Diagnose gestellt und die Therapie basiert auf der Art und Schwere des AV-Blocks sowie dem hämodynamischen Status der Betroffenen.
Schenkel- und Hemiblöcke treten auf, wenn die physiologische elektrische Aktivität im His-Purkinje-System gestört oder unterbrochen ist. Es existieren unterschiedliche Genesen, die die Struktur des Herzens und/oder des Reizleitungssystems direkt beeinflussen können (z. B. Myokardischämie, Myokarditis Myokarditis Myokarditis, Kardiomyopathie Kardiomyopathie Kardiomyopathien: Übersicht & Vergleich). Obwohl sie in der Regel asymptomatisch sind, können Schenkel- und Hemiblöcke gelegentlich auch zu Synkopen führen.
Antiarrhythmika werden verwendet, um Herzrhythmusstörungen zu behandeln. Für die Therapie tachykarder Herzrhythmusstörungen stehen nach Einteilung nach Vaughan Williams vier Medikamentenklassen zur Verfügung (die Einteilung wird kritisch diskutiert, da sich nicht alle Medikamente eindeutig zuordnen lassen):