B-Lymphozyten, auch B-Zellen genannt, sind wichtige Bestandteile des adaptiven Immunsystems. Im Knochenmark Knochenmark Knochenmark: Zusammensetzung und Hämatopoese durchlaufen sie von hämatopoetischen Stammzellen ausgehend eine Reihe von Entwicklungsschritten, um zu reifen, naiven B-Zellen zu werden. Die Zellen migrieren zur Aktivierung und weiteren Proliferation zu sekundären lymphatischen Organen. Die Aktivierung erfolgt durch eine Antigenstimulation mit oder ohne Hilfe von T-Zellen T-Zellen T-Zellen. Bei T-Zell-unabhängiger Aktivierung durch Antigene wie bakteriellen Lipopolysaccariden kann eine kurzweilige, durch Plasmazellen vermittelte Immunantwort beobachtet werden. Die T-Zell-abhängige Aktivierung T-Zell-abhängige Aktivierung Humorale Mechanismen des erworbenen Immunsystems hingegen führt zu einer Differenzierung sowohl zu Plasmazellen als auch zu Gedächtniszellen Gedächtniszellen Erworbene Immunantwort. Aktivierte B-Zellen vermehren sich infolgedessen in den Keimzentren, wenn auch nicht alle am Ende zu Effektor-B-Zellen differenzieren. Durch somatische Hypermutation durchlaufen B-Zellen einen weiteren Mechanismus, um die Affinität des Antikörpers zum Antigen zu erhöhen. Nur diejenigen B-Zellen mit hochaffinem B-Zell-Rezeptor erreichen eine terminale Differenzierung. Mithilfe von Zytokinen vollziehen B-Zellen einen Klassenwechsel von IgM zu einem anderen Ig-Isotyp. Nach dem Klassenwechsel differenzieren sie zu Plasmazellen (die Antikörper produzieren) oder Gedächtniszellen Gedächtniszellen Erworbene Immunantwort (die für eine verbesserte sekundäre Immunantwort bei Reinfektion sorgen).
Kostenloser
Download
Lernleitfaden
Medizin ➜
B-Lymphozyten (“B” für Bursa Fabricii, dem bei Vögeln erstbeschriebenen primären lymphatischen Organ) oder B-Zellen sind eine Gattung von Lymphozyten Lymphozyten Lymphozyten, die aus dem gemeinsamen lymphatischen Progenitorzellen hervorgehen.

Der B-Zell-Rezeptor (BCR) besteht aus einem Ig-Molekül und einem Signalmolekül:
Ig besteht aus 2 identischen schweren Ketten und 2 identischen leichten Ketten, die durch eine Disulfidbrücke verbunden sind. Das membranständige Ig ist an der Zelloberfläche verankert.
Um ihre Funktionalität zu erlangen, durchläuft die B-Zelle Entwicklungsstadien im Knochenmark Knochenmark Knochenmark: Zusammensetzung und Hämatopoese und den sekundären lymphatischen Organen:
| Reifephase | Ig-Gene | B-Zell-Rezeptor (BCR) | Assoziierte Entwicklungsschritte |
|---|---|---|---|
| Antigen-unabhängig | |||
| Frühe Pro-B-Zelle | Keimbahn-DNA | Keiner | Keine Expression schwerer oder leichter Ketten |
| Pro-B-Zelle | DJ-Umlagerung der IGH | Keiner | Beginn der Expression von CD19, CD34 und HLA-DR (MHC-Klasse-II-Zelloberflächenrezeptor) |
| Pre-B-Zelle | VDJ-Umlagerung der IGH abgeschlossen | Bildung Pre-BCR:
|
Bildung weiterer Oberflächenmarker (darunter CD79, CD10, CD20, CD40 und die terminale Desoxyribonukleotidyltransferase) |
| Unreife B-Zelle |
|
Reifer BCR (IgM-Molekül) | Fortsetzung der Expression von HLA-DR, CD19, CD20 und CD40, jedoch nicht die der weiteren Marker (z.B. CD10, CD34 und terminalen Desoxyribonukleotidyltransferase) |
| Reife B-Zelle (naiv) |
|
Wenn mit reifem BCR (IgM) → Verlassen des Knochenmarks | CD19 und CD20 vollständig exprimiert |
| Antigen-abhängig | |||
| Reife B-Zelle (in sekundären lymphatischen Organen) | Reifes BCR (Expression von IgM und IgD, sobald einmal innerhalb des sekundären lymphatischen Organs) | Zellen entweder in Ruhe oder B-Zell-Aktivierung: Interaktion der B-Zellen mit exogenen Antigen- und/oder T-Helferzellen | |
| Aktivierte B-Zelle | Klassenwechsel | Nach Aktivierung Wechsel zu IgE, IgG, IgA oder Verbleib als IgM | |
| B-Gedächtniszelle |
|
||
| Plasmazelle |
|
||

Differenzierungsstufen der B-Zelle:
Die B-Zell-Produktion beginnt in Antigen-unabhängigen Stadien mit der hämatopoetischen Stammzelle, die sich zu einer lymphatischen Progenitor-Zelle und dann zu einer Pro-B-Zelle sowie Prä-B-Zelle oder auch B-Vorläuferzelle wird. Während der nächsten Schritte erfolgt eine Genumlagerung, um das Ig-Molekül zusammenzusetzen. Schwere Ketten des Ig werden als Erstes in der Diversitäts- und Joining-Region umgeordnet, um die Pro-B-Zelle zu bilden. Im nächsten Schritt (Prä-B-Zelle) wird die Genumlagerung der schweren Ketten des Ig (Variable, Diversitäts- und Joining-Region) abgeschlossen und der Prä-B-Zell-Rezeptor gebildet. Es folgt die Umlagerung der Gene der leichten Ketten (Kappa [κ] oder Lambda [λ]), die zur Expression eines vollständigen IgM-Antikörpermoleküls einer unreifen B-Zelle führt. Anschließend wird eine reife B-Zelle (naiv) sowohl mit IgM als auch mit IgD gebildet.
Antigen-abhängige Stadien finden in sekundären lymphatischen Organen statt. Sobald die reifen B-Zellen IgM und IgD produzieren, kann ein Klassenwechsel stattfinden, um IgE, IgG und IgA herzustellen. B-Zellen werden aktiviert und differenzieren zu Plasmazellen oder Gedächtniszellen.
Die B-Zelle wandert vom Knochenmark Knochenmark Knochenmark: Zusammensetzung und Hämatopoese zu den sekundären lymphatischen Organen. Es ist eine Reihe von Schritten erforderlich, um eine immunkompetente, differenzierte B-Zelle herzustellen: Aktivierung durch ein Antigen, Proliferation, Affinitätsreifung, Klassenwechsel und Differenzierung (zu Plasma- oder Gedächtniszellen Gedächtniszellen Erworbene Immunantwort).

Histologischer Schnitt eines Lymphknotens mit Kortex, Parakortex und Medulla
Bild von Geoffrey Meyer, bearbeitet von Lecturio.
Aufbau und funktionelle Regionen eines Lymphknotens, bestehend aus einer kollagenreichen Bindegewebskapsel und einem darunter liegenden subkapsulären Sinus.
Die zellulären Bestandteile können auf den Kortex (1), bestehend aus B-Zellen, follikulären T-Helfer-Zellen und follikulären dendritischen Zellen, die in primären Follikeln angeordnet sind, in denen B-Zellen Antigene erkennen, die ein follikuläres Netzwerk dendritischer Stromazellen präsentiert werden, und den Paracortex (2) mit T-Zellen, dendritische Zellen und fibroblastische Retikulumzellen, die das Netzwerk der Stromazellen und retikuläre Fasern bilden, aufgeteilt werden.
Das innere Mark besteht aus lymphatischem Gewebe (Marksträngen), das von Lymphe führendem Marksinus durchzogen wird.
Die B-Zell-Aktivierung durch Antigenpräsentation kann auf unterschiedlichen Wegen erfolgen:

B-Zell-Aktivierung (T-Zell-abhängig):
Interaktion zirkulierenden Antigens mit dem BCR der B-Zelle. Endozytose, Fragmentierung des Antigens und Präsentation der Peptidfragmente über MHC-Klasse-II-Molekülen auf der Zelloberfläche. Follikuläre T-Helferzellen (Tfh) (spezialisierte CD4+-T-Helferzellen) erkennen und binden den Antigen-MHC-II-Komplex. Zytokinfreisetzung aus den Tfh-Zellen, was zur Aktivierung und Proliferation der B-Zellen führt. Aktivierte B-Zellen dringen in die Keimzentren ein, wo sie ihren Entwicklungsprozess fortsetzen und differenzieren.
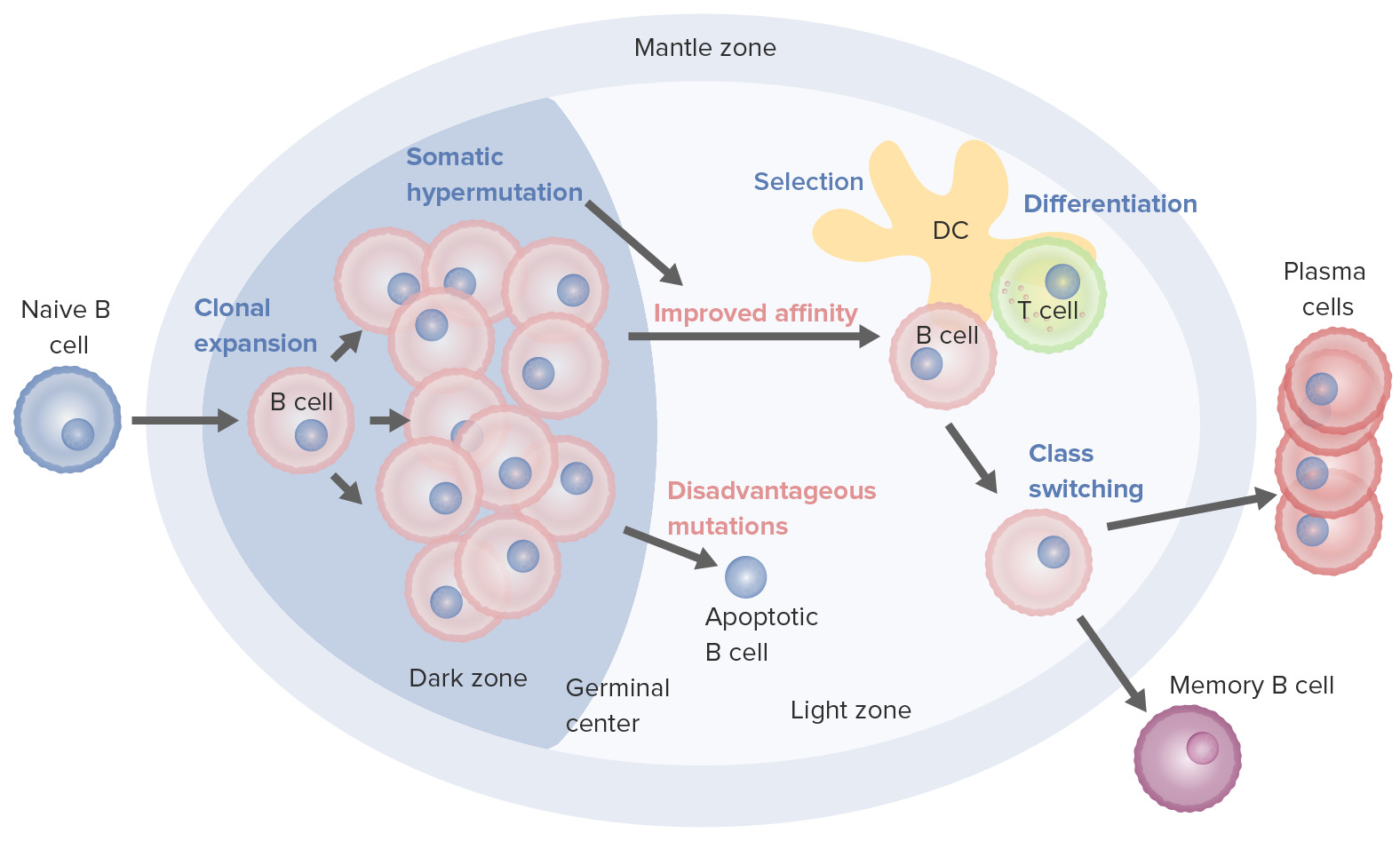
B-Zell-Aktivierungs- und Reifungsprozesse im Keimzentrum:
Bei Aktivierung bewegt sich die B-Zelle aus der Mantelzone und dringt in das Keimzentrum ein. Die B-Zell-Proliferation (klonale Expansion) findet statt und die Antikörperaffinität zum Antigen wird durch den Prozess der somatischen Hypermutation erhöht. Wiederholte Zyklen der Proliferation und Hypermutation verfeinern den B-Zell-Rezeptor. Allerdings differenzieren nicht alle B-Zellen weiter, insbesondere wenn die Affinität schwach ist. Sie gehen in Apoptose, wenn die Antigen-Antikörper-Bindung nicht optimiert worden ist. Diejenigen mit starker Affinität überleben (Selektion) durch Überlebenssignale follikulären dendritischen Zellen (FDC) und T-Zellen. Diese selektierten B-Zellen gehen zum Klassenwechsel und Differenzierung in Plasma- oder Gedächtniszellen über.

Keimzentrum: Histologie des Keimzentrums eines sekundären lymphatischen Gewebes
LZ: Lichtzone
DZ: dunkle Zone

Zusammenfassung der B-Zell-Entwicklung bis zur Differenzierung (vom Knochenmark zum sekundären lymphatischen Organ):
B-Zell-Entwicklung:
Im Knochenmark entwickeln sich B-Zellen, dadurch, dass sie einen B-Zell-Rezeptor (BCR) ausprägen, zu unreifen B-Zellen. Danach Migration in sekundäre lymphatische Organe, wo eine Aktivierung stattfindet.
B-Zell-Aktivierung:
Ein Antigen bindet die B-Zelle mit dem am besten passenden BCR. Ein Aktivierungsweg ist T-Zell-unabhängig, wobei die aktivierte B-Zelle ohne Hilfe der T-Zelle dazu gebracht wird, sich in eine kurzlebige Plasmazelle (Antikörperproduktion) zu differenzieren. Bei der T-Zell-abhängigen Aktivierung erkennt die T-Zelle den Antigen-MHC-Klasse-II-Komplex und löst damit die Proliferation der B-Zelle im Keimzentrum des sekundären lymphatischen Gewebes aus.
Proliferation und Reifung:
Dem Aktivierungsprozess folgt die somatische Hypermutation (eine genetische programmierte Mutation zur Affinitätssteigerung des Antikörpers zum Antigen). Wiederholte Zyklen von Proliferation und Hypermutation verfeinern den BCR. Diejenigen B-Zellen mit der besten Affinität werden selektiert und überleben; diejenigen mit geringer Affinität gehen in Apoptose. Die überlebenden B-Zellen durchlaufen dann einen Klassenwechsel, bei dem der Aufbau der schweren Kette mithilfe von Zytokinen verändert wird (Wechsel von IgM zu anderen Isotypen).
Differenzierung:
Diese B-Zellen differenzieren sich dann in Plasmazellen und Gedächtniszellen und verlassen das Keimzentrum.
Unterschiedliche Prozesse ermöglichen es dem Menschen, ausgehend von der anfänglichen B-Zell-Produktion deutlich mehr verschiedene Antikörpermoleküle zu produzieren als dafür Gene im Genom Genom Grundbegriffe der Genetik vorliegen.
Es wird geschätzt, dass Milliarden von Antikörpern erzeugt werden können. In Relation dazu kodieren etwa 30.000 Gene für Antikörper.
Einzigartige Mechanismen erzeugen Diversität: